Unser Mikrobiom: Wir sind nicht allein
auch: Darmflora / mikrobielle Darmbesiedelung / Darmsymbiose / Intestinalflora
Schon lange ist bekannt, dass wir Menschen nicht nur aus Zellen bestehen. Wir beherbergen auf unseren Körperoberflächen Unmengen kleinster Lebewesen – die meisten davon sind Bakterien – denen wir bislang nur wenig Aufmerksamkeit geschenkt haben. Erst im vergangenen Jahrzehnt ist das Mikrobiom, vor allem das des Darmes, in den Fokus des wissenschaftlichen Interesses gerückt. Selbst der Begriff „Mikrobiom“ ist noch ganz frisch, denn früher sprach man einfach von der „Darmflora“, bis Joshua Lederberg im Jahr 2001 den Begriff Mikrobiom einführte. Welchen Einfluss die neu gewonnenen Erkenntnisse bereits heute und in den kommenden Jahren auf unsere Gesundheit und auf die Behandlung und Vorbeugung von Krankheiten haben, erfahren Sie auf dieser Seite.
Von Dr. Evelyn Zientz
Auf dieser Seite:
› Mikrobiom bei Reizdarm
› Dünndarmfehlbesiedelung (SIBO)
› Pseudomembranöse Colitis
› Mikrobiom und Übergewicht
› Diabetes und Mikrobiom
› Endotoxine und stille Entzündungen
› Autoimmunerkrankungen
› Psychische und neurologische Erkrankungen
› Mikrobiom und Atherosklerose
› Mikrobiom und Krebsentstehung
Forschungsfeld Darmflora
Moderne molekularbiologische Methoden machen es heute möglich, die Gesamtheit der mit uns assoziierten Lebewesen zu erfassen. Dank Hochdurchsatz-Sequenzierungen von amplifizierten Markergenen, klassischerweise 16S-rRNA, ist es möglich, die Artenvielfalt des Lebensraumes „Mensch“ zu erfassen. Und er ist weit artenreicher, als man bisher angenommen hatte.
Das Darmmikrobiom ist ein junges Forschungsfeld. und die Wissenschaft wurde erst im vergangenen Jahrzehnt auf die enorme Artenvielfalt und Diversität des menschlichen Mikrobioms aufmerksam, das einige Wissenschaftler sogar als eigenständiges Organ bezeichnen.
Große Artenvielfalt – geringes Krankheitsrisiko
Es treten immer mehr Zusammenhänge zwischen einem Ungleichgewicht im Darm-Mikrobiom und verschiedensten – heute leider alltäglichen – Krankheiten zu Tage. Chronisch entzündliche Darmerkrankungen, Diabetes, Fettleibigkeit, aber auch psychische oder neurologische Erkrankungen gehen oft mit Veränderungen des Darm-Mikrobioms einher. Aber gibt es zwischen diesen Korrelationen auch einen ursächlichen Zusammenhang? Vermutlich schon, denn viele Krankheiten lassen sich mit den Mikroben im Darm von einem Individuum auf ein anderes übertragen, wie in Studien mehrfach gezeigt wurde. Für Gesundheit und Wohlbefinden gilt es also, das persönliche Mikrobiom in einem optimalen Zustand zu halten.
Eine große Artenvielfalt ist dabei sehr wichtig, denn viele Erkrankungen gehen mit einer reduzierten Anzahl der vertretenen Spezies einher.
Faktor Ernährung
Wie Studien zeigen, profitiert die Artenvielfalt von einer vollwertigen, ballaststoffreichen Ernährung. Unsere moderne, westliche Ernährung, die sehr fett- und eiweißreich ist, dafür aber wenig Ballaststoffe enthält, lässt das Mikrobiom an Arten verarmen. Wer sich bewusst ist, wie wichtig ein gesundes Mikrobiom für das eigene Wohlbefinden ist, wird sicher darauf achten, dass die kleinen Mitbewohner und Lebenskameraden keinen Hunger leiden müssen.

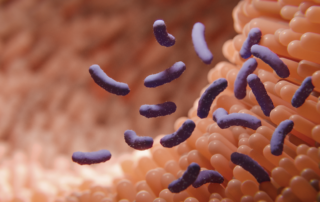
Foto: Wir sind nicht allein: Der Darm beherbergt eine Vielzahl von Mikroben, die in ihrer Gesamtheit als Mikrobiom (früher: Darmflora) bezeichnet wird. Bildnachweis: adobe media, woman take intestine board, von Ryanking 999
Ökosystem Mensch
Jedes Lebewesen, also auch der Mensch, ist von winzigen Mikroorganismen besiedelt. Und wir besitzen viele Oberflächen – nicht nur die äußerlich sichtbaren -, auf denen die Besiedelung stattfindet. Ein Säugetier ist vereinfacht dargestellt wie ein Rohr mit einer äußeren und einer inneren Oberfläche. Man kann sich vorstellen, dass der eigentliche Körper, also die Gesamtheit der Organe, das Material darstellt, aus dem das Rohr besteht. Die äußere Oberfläche ist die Haut, die innere Oberfläche bildet die Darmwand. Die Darmwand ist eine stark aufgefaltete Schleimhaut. Eine Schleimhaut ist eine Haut ohne Haare und ohne Hornschicht, die aus den verschiedensten Gründen Schleim produziert.
Unser Darm ist besonders dicht von Mikroorganismen besiedelt. Bakterien machen dabei den größten Anteil von 99% aus. Aber vereinzelt kommen auch Pilze, Viren und Protozoen, also einzellige Tierchen, vor.
Nach neuesten Schätzungen besitzt der „Standardmensch“ (männlich, 1,70 m groß, 30 Jahre, 70 kg) etwa 30 Billionen Zellen und trägt 38 Billionen (das ist eine 10 mit 12 Nullen) mikrobielle Untermieter mit sich herum.
Die geschätzten 1,5 kg Mikrobenmasse im Darminhalt machen etwa 0,3% seines Körpergewichts aus. Da fällt es schwer sich vorzustellen, dass wir mit unseren Mikroben einfach so nebeneinander her leben, ohne gegenseitig Einfluss zu nehmen. Und so ist es auch nicht.
 Grandiose Artenvielfalt
Grandiose Artenvielfalt
Unser Darm ist ein Ökosystem, das sehr vielen verschiedenen Spezies einen Lebensraum bietet. Bisher wurden weit über 1000 – nach neuesten Studien sogar 35 000 – verschiedene Arten im menschlichen Darminhalt entdeckt. Aber wir beherbergen davon nicht alle. Unser persönliches Mikrobiom besteht aus etwa 150 bis 200 verschiedenen Arten. Das erlaubt sehr viel individuelle Variationen und damit ist unser Mikrobiom beinahe so unverwechselbar wie ein Fingerabdruck.
Jede dieser Arten verfügt über ihr eigenes Genom und durch die enorme Artenvielfalt ist der Informationsgehalt des gesamten Mikrobioms, gemessen an der Anzahl der darin enthaltenen Gene, mindestens um den Faktor 100 höher als der unseres eigenen Erbgutes. Es wird deshalb auch als zweites Genom bezeichnet. Das sind enorme Ressourcen, auf die wir hier zurückgreifen können. Denn unser eigenes Erbgut variiert nur um etwa 0,1%. Das bakterielle dagegen um mehr als 50%.
Der Einfluss des Mikrobioms ist groß und die Varianz der mikrobiellen Aktivität ebenfalls. Es zeigt sich, wie wichtig es für Gesundheit und Wohlbefinden ist, die „richtigen“ Mikroben im Darm zu beherbergen.
Entwicklung des Mikrobioms
Früher glaubte man, der erste Kontakt eines Menschen mit Bakterien fände während der Geburt statt. Heute weiß man, dass schon das Fruchtwasser Bakterien enthält und ein ungeborenes Kind schon im Mutterleib mit Bakterien in Kontakt kommt. Die erste Besiedlung des Darms erfolgt über das Fruchtwasser. Das muss nicht immer gut sein. Es ist nicht ausgeschlossen, dass bestimmte Bakterien dieser sehr frühen Besiedelung für Frühgeburten mitverantwortlich sein könnten.
Übertragung von Geburtsform abhängig
Die wichtigste Begegnung mit der zukünftigen Darmflora findet während der Geburt statt. Für die Besiedlung des Darmes stehen verschiedene Inokuli (infektiöse Materialien) zur Verfügung, je nachdem wie die Entbindung erfolgt. Bei einer Vaginalgeburt trifft das Neugeborene zuerst auf die Vaginalflora und nimmt Bifidobacterium-, Bacteroides- und Lactobacillus-Arten auf. Bei einem Kaiserschnitt trifft das Neugeborene auf die Bakterienflora der Haut und des Operationssaales. Es wird mit Clostridien und nicht klassifizierten Enterobakterien Bekanntschaft machen.
Eine natürliche Geburt ist eine gute Voraussetzung, ein artenreiches Mikrobiom und damit ein gesundes angeborenes Immunsystem zu entwickeln. Ein Kaiserschnitt birgt für das Kind ein erhöhtes Risiko später an Asthma, Typ-1-Diabetes, Fettleibigkeit oder Zöliakie zu erkranken.
Muttermilch vs. Kuhmilch
Wie sich das junge Mikrobiom weiter entwickelt hängt stark von der Ernährung seines Wirtes ab. Babys, die gestillt werden nehmen täglich eine ordentliche Portion Bakterien, vor allem Lactobacillus, Staphylococcus, Enterococcus und Bifidobacterium mit der Muttermilch auf. Die Muttermilch sorgt auch dafür, dass die „richtigen“ Bakterien sich im Darm des Säuglings ansiedeln. Sie enthält Antikörper gegen schädliche Bakterien und spezielle Oligosaccharide, die präbiotisch wirken, also den guten Bakterien als Futter dienen.
Das Mikrobiom von Säuglingen, die mit Flaschenmilch ernährt werden, unterscheidet sich von dem gestillter Babys. Bei gestillten Babys dominieren Bifidobacterium und Lactobacillus während Flaschennahrung Enterococcus, Enterobacteria, Bacteroides, Clostridia fördert. Muttermilch enthält für den Menschen unverdauliche Oligosaccharide, (HMO), die in Kuhmilch fehlen. Sie dienen den Bakterien als Nahrung. Insgesamt hat der Modus der Geburt aber einen größeren Einfluss auf die Zusammensetzung der Bakterienpopulation als die Ernährung.
Auch eine Antibiotikabehandlung im sehr frühen Kindheitsstadium kann die Zusammensetzung des Mikrobioms nachhaltig verändern. Im Laufe der ersten zwei Lebensjahre reift die Darmflora heran und im Alter von etwa drei Jahren entspricht das Mikrobiom des Kindes dem eines Erwachsenen.
Zusammensetzung des Mikrobioms
Dominierende Bakteriengruppen des menschlichen Darm-Mikrobioms
Das Mikrobiom jedes einzelnen von uns ist einzigartig. Aber trotz der Artenvielfalt und der damit verbundenen Vielzahl an möglichen Zusammenstellungen des Mikrobioms kommen immer wieder die selben charakteristischen Arten vor. Unsere Darmflora wird von nur wenigen Bakteriengruppen dominiert:
- Firmicutes (z.B. Laktobazillen, Clostridien, Ruminokokken)
- Bacteroidetes (z.B. Prevotella, Bacteroides)
- Actinobakterien (z.B. Bifidobakterien)
- Proteobakterien (z.B. Escherichia coli)
Dabei stellen Firmicutes und Bacteroidetes mit über 90% der Darmbakterien die mit Abstand größte Gruppe.

Abbildung: Dominierende Bakteriengruppen des menschlichen Darm-Mikrobioms: Firmicutes, Bacteroidetes, Actinobakterien, Proteobakterien (c) fruhimi.de, Original: Adobe Media, Maria Nechaeva
Enterotypen des Mikrobioms
Unter den möglichen Varianten des Mikrobioms fallen drei verschiedenen Gruppierungen auf, die immer wieder in ähnlicher Form auftreten. Man bezeichnet sie als Enterotypen.
Enterotyp 1:
Beim Enterotyp 1 dominieren Bakterien der Gattung Bacteroides. Diese Bakterien verfügen über ein hohes saccharolytisches und proteolytisches Potenzial und beziehen ihre Energie aus dem Stoffwechsel von Proteinen und Kohlenhydraten. Dieser Enterotyp dominiert bei Menschen, die sich eiweiß- und fettreich ernähren.
Enterotyp 2:
Bei diesem Typ der Darmflora ist Prevotella die vorherrschende Bakterienart. Prevotella gehört ebenfalls zum Stamm der Bacteroidetes und ist mit Bacteroides nah verwandt. Dieser Enterotyp herrscht bei Menschen vor, die sich überwiegend von Kohlenhydraten und Einfachzuckern ernähren. Pevotella kann die Darmschleimhaut angreifen, indem sie deren Glycoproteine abbaut. Ob Prevortella gut oder böse ist, ist daher noch unklar, da verschiedene Stämme der gleichen Art unterschiedliche Aktivitäten entwickeln.
Enterotyp 3:
Dieser Enterotyp ist durch das Vorherrschen der Gattung Ruminococcus gekennzeichnet. Ruminokokken bauen hochmolekulare Kohlenwasserstoffe ab und vergären sie zu kurzkettigen Fettsäuren, die eine wichtige Energiequelle für die Epithelzellen der Darmschleimhaut darstellen. Allerdings können sie die Darmschleimhaut auch angreifen und Mucine abbauen. In der Regel überwiegt aber der positive Effekt und Ruminokokken sind Indikatorbakterien für ein gesundes Mikrobiom.
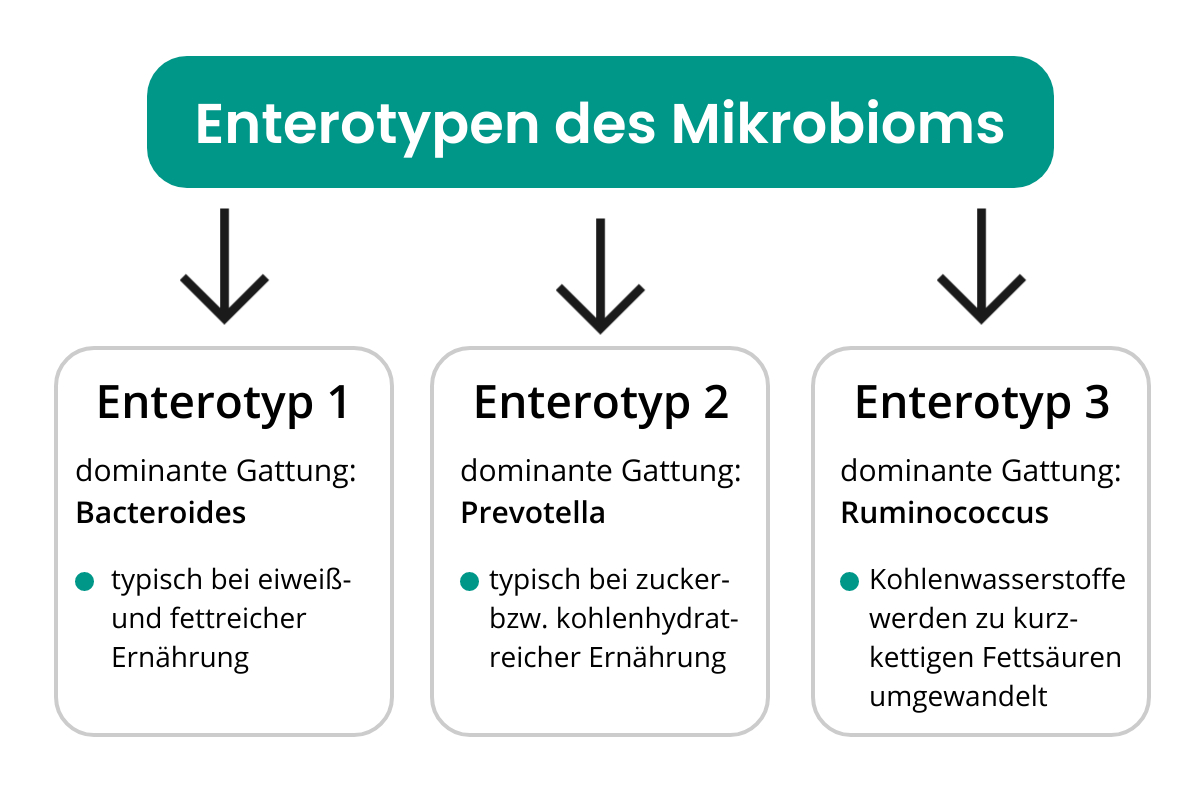
Abbildung: Enterotypen des menschlichen Mikrobioms, (c) fruhimi.de
Lokale Verteilung der Bakterien
Die Bakterien sind nicht zufällig im Darm verteilt. Die Zusammensetzung der Bakteriengesellschaft verändert sich sowohl längs, mit dem Verlauf des Verdauungssystems als auch axial. Der Großteil der Darmbakterien siedelt im Dickdarm. Während in der Speiseröhre etwa 10¹-10² Bakterien pro Gramm Biomasse, hauptsächlich Streptokokken, vorkommen, sind es im Dünndarm 10³, im Dickdarm 10¹² Zellen pro Gramm Darminhalt.
Auch im Querschnitt ist die Bakterienbesiedelung des Darms nicht homogen. Manche Arten, wie Vertreter der Gattungen Bacteroides, Bifidobacterium, Streptococcus, Enterobacteriacae, Enterococcus, Clostridium, Lactobacillus and Ruminococcus halten sich bevorzugt im Lumen des Darms auf. Sie sind auch leicht im Stuhl nachweisbar. Andere, wie Clostridium, Lactobacillus, Enterococcus und Akkermansia besiedeln die Mucosa und sind nicht so leicht zu entdecken.

Abbildung: Quantitative Bakterienverteilung in Gramm pro Biomasse in Speiseröhre, Dünndarm, Dickdarm. (c) fruhimi.de, Adobe Media, Originalbild v. Crystal light
Bakteriengruppen im Überblick
Eine gesundes Mikrobiom zeichnet sich in jedem Fall durch eine dichte Besiedlung mit Firmicutes und Bacteroidetes aus, gefolgt von Actinobakterien und Verrucomicrobia. Andere Gruppen, wie Proteobakterien, sollten dagegen nicht so häufig vorkommen.
- Firmicutes sind – wie ihr Name schon andeutet – die Dickhäuter unter den Bakterien, denn wörtlich übersetzt bedeutet firmus „stark“ und cutis „Haut“. Zu ihnen gehören zum Beispiel die Ruminokokken, die typisch für den Enterotyp 3 sind.
- Bacteroidetes stellen einen Stamm im Reich der Bakterien dar, zu dem auch die für Enterotyp 1 und 2 charakteristischen Arten Bacteroides und Prevotella gehören.
- Zu den Actinobakterien zählt die Gattung Bifidobacterium, die der Hauptproduzent von Folsäure im Darmtrakt ist. Bifidobakterien sind enorm nützliche, gutwillige und deshalb sehr willkommene Darmbewohner.
- Proteobakterien sind eine vielgestaltete Gruppe von Bakterien, die unter dem Mikroskop die unterschiedlichsten Erscheinungsformen aufweisen können, deren Verwandtschaft aber anhand ähnlicher Nukleinsäurestrukturen offengelegt wurde. Sie sind also genetisch verwandt. Zu ihnen zählen auch die Enterobakterien, wie Escherichia coli. Sie gehören zur normalen Darmflora, machen aber nur einen geringen Anteil der Population aus.
Zu guter Letzt sind Verrucomicrobia durch die Art Akkermansia muciniphilia vertreten. Diese Bakterien sind wichtig für den Schutz der Darmschleimhaut, stellen aber maximal 5% der Bakterienmasse der Darmflora. Sie zählen damit nicht zu den dominierenden Vertretern der Darmflora.
Aufgaben des Mikrobioms
Unterstützung der Verdauung
Die Symbionten im Darm leben hauptsächlich von der Fermentation von Kohlenhydraten, die der Wirt entweder übrig gelassen hat oder die für ihn unverdaulich sind, so genannte Ballaststoffe. Bacteroides und Bifidobacterium, aber auch die möglicherweise problematischen Enterobakterien vergären sie zu kurzkettigen Fettsäuren (SCFA, short chain fatty acid) wie Butyrat, Propionat oder Acetat. Diese Fettsäuren sind gute Energiequellen für den Wirt. Man geht aber auch davon aus, dass die Energiehomöostase des Wirtes, also das Sättigungsgefühl, durch SCFAs reguliert wird.
Die Darmbakterien fördern auch die Fettverdauung, indem sie die Fett verbrennenden Enzyme der Fettzellen aktivieren. Bacteroides steigert die Verdauung von Fett, indem es die Gene für den Fettstoffwechsel aktiviert.
Das Darm-Mikrobiom ist auch stark am Proteinstoffwechsel beteiligt. Bakterielle und Wirtsenzyme, Proteinasen, die Proteine in kleinere Abbauprodukte, die Peptide, zerlegen und Peptidasen, die wiederum die Peptide abbauen, wirken hier zusammen. So werden Eiweißstoffe in ihre einzelnen Bausteine, die Aminosäuren zerlegt.
Die Bakterien verfügen über zahlreiche Transportproteine, mit denen sie die Aminosäuren aufnehmen. Anschließend bilden sie daraus kleine Signalmoleküle, wie GABA (Gamma-aminobuttersäure, ein Neurotransmitter) oder Histamin, ein Gewebshormon, und antimikrobiell wirksame Peptide, so genannte Bakteriozine.
 Sekundäre Pflanzenstoffe
Sekundäre Pflanzenstoffe
Neuere Studien zeigen, dass unsere Darmbakterien auch am Abbau verschiedener Polyphenole beteiligt sind. Polyphenole sind sekundäre Pflanzenstoffe, denen vor allem eine antioxiative Wirkung zugeschrieben wird. Diese Polyphenole liegen zunächst in einer inaktiven, an verschiedene Zucker gebundenen Form vor.
Die Bakterien spalten die Zuckerreste ab und aktivieren dadurch die Pflanzenstoffe, worauf sie ihre gesundheitsfördernde Wirkung entfalten können.
Stabilisierung der Darmbarriere
Im Augenblick mehren sich die Hinweise, dass die Darmbakterien an der Aufrechterhaltung der Struktur und Funktion der Darmbarriere beteiligt sind. Die Epithelzellen der Darmschleimhaut sind durch besonders stabile Zellkontakte, Desmosomen und Tight Junctions, fest miteinander verbunden.
Bestimmte Oberflächenstrukturen des „guten“ Darmbakteriums Bacteroides können helfen, diese Zellkontakte zu festigen. Ein anderes Bakterium der Gattung Lactobacillus kann die Apoptose, also den programmierten Zelltod, der Epithelzellen der Darmschleimhaut verhindern, indem es Proteine in die Umgebung abgibt, die entsprechende Signalübertragungswege steuern.
Darmbakterien modulieren auch das Endocannabinoid System. Das Endocannabinoid System ist ein Teil des Nervensystems, das aus Cannabinoid-Rezeptoren und ihren natürlichen Bindungspartnern besteht. Wird es aktiviert, startet es eine Signalübertragung, deren Auswirkung auf das Gehirn noch nicht vollkommen verstanden ist. Da auch das Rauschgift Cannabis dieses System aktiviert, ist von einer positiven Wirkung bzw. Empfindung auszugehen.
Überraschenderweise sind alle Komponenten des Endocannabinoid-Systems auch im Darmgewebe vorhanden. Man weiß, dass das Endocannabinoid-System an der Steuerung verschiedener Vorgänge im Gastrointestinaltrakt beteiligt ist, etwa der Regulation der Peristaltik, sensorischen Vorgängen oder auch daran, das Darmepithel intakt zu halten.
Genau genommen regulieren Bakterien die Funktion der Darmbarriere über das Endocannabinoid-System, indem sie die Konzentration körpereigener – oder in diesem Fall bakterieller – Endocannabinoide erhöhen und das System aktivieren.
Als Folge sinkt die Konzentration von Endotoxinen. Und Endotoxine wiederum sind Bruchstücke bakterieller Zelloberflächen, die, wenn sie in den Körper gelangen, als Auslöser verschiedenster Beschwerden infrage kommen.
Das Mikrobiom trägt auch zum strukturellen Aufbau der Mucosa (Darmschleimhaut) bei, indem es die über die Aktivierung des Transkriptionsfaktors Angiogenin die Neubildung von Kapillaren im Darmgewebe fördert und damit für optimale Blutversorgung und Stoffaustausch sorgt.
 Immunmodulation
Immunmodulation
Eine wichtige Aufgabe des Mikrobioms ist die Modulation des Immunsystems. Aufgabe des Immunsystems ist unter anderem, den Körper vor Schäden durch bakterielle oder virale Krankheitserreger zu schützen. Es ist im Körper in verschiedenen Geweben zu finden: Im Blut, im Lymphsystem, in der Milz, im Knochenmark und in den Zellzwischenräumen. Aber wo wären die Zellen des Immunsystems besser aufgehoben, als direkt an der Oberfläche? Auch das Innere des Verdauungskanals zählt medizinisch betrachtet zur „Außenwelt“, ist also eine Oberfläche. Der Magen-Darm-Trakt, der durch die aufgenommene Nahrung besonders häufig mit Keimen und Fremdkörpern in Kontakt kommt, bietet mit seinen 400 – 500 m² Oberfläche dem Immunsystem daher einen großen und wichtigen Wirkungskreis.
GALT und Pleyer-Plaques
Die Darmschleimhaut enthält lymphoidales Gewebe, genauer Schleimhaut assoziiertes Lymphgewebe (GALT, gut associated lymphoid tissue). Vor allem im Gewebe des Ileums, dem unteren Teil des Dünndarms, sind einzelne Lymphozyten oder Verbände davon im Form vom Lymphfollikeln oder Peyer-Plaques, die wiederum Ansammlungen von Lymphfollikeln sind, vorhanden.
Lymphozyten und Darmschleimhaut
Lymphozyten sind weiße Blutkörperchen, deren Aufgabe es ist, Fremdkörper wie Bakterien oder Viren zu erkennen und deren Eliminierung einzuleiten. Zu diesem Zweck produzieren sie Antikörper und setzen Botenstoffe, sogenannte Zytokine, frei, die wiederum andere unterstützende Immunzellen aktivieren. Mehr als siebzig Prozent der körpereigenen Immunzellen befinden sich in der Darmschleimhaut. Und über neunzig Prozent der Antikörper werden dort gebildet.
Das Immunsystem hat im Darm nun die schwierige Aufnahme, zwischen guten und schlechten Bakterien, also möglichen Pathogenen, zu unterscheiden und potentielle Krankheitserreger zu entfernen.
Die Wächterfunktion dendritischer Zellen
Ein bestimmter Typ der Lymphozyten, die dendritischen Zellen, spielt hier eine wichtige Rolle. Diese Zellen verfügen über feine Fortsätze, die Dendriten, mit denen sie in das Lumen des Darms hineinlangen und ersten Kontakt mit unbekannten, fremdartigen Strukturen aufnehmen. Sie sind Antigen präsentierende und Antigene produzierende Zellen, die sich mit ihrer Information auf den Weg zu den Lymphknoten machen und dort eine Immunantwort auslösen.
Aber wie wird entschieden, ob ein Fund nun gefährlich ist oder nicht? Das hängt vermutlich vom Kontext ab, in dem das Antigen gebildet wurde. Die dendritischen Zellen bilden so genannte co-stimulatorische Moleküle. Wenn nun das Epithel der Schleimhaut geschädigt ist, bilden sie besonders viel davon, was eine Immunantwort wahrscheinlicher macht. Dann kann es davon ausgehen, dass ein Erreger schon in die Schleimhaut eingedrungen ist und entfernt werden muss.
Das Mikrobiom, also unsere Darmflora, ist an der Entwicklung eines gut funktionierenden, schleimhaut-assoziierten Lymphgewebes (GALT) beteiligt. Es hat Einfluss auf die Entwicklung der Peyers-Plaques und steuert die Bildung der „richtigen“ Immunglobuline.
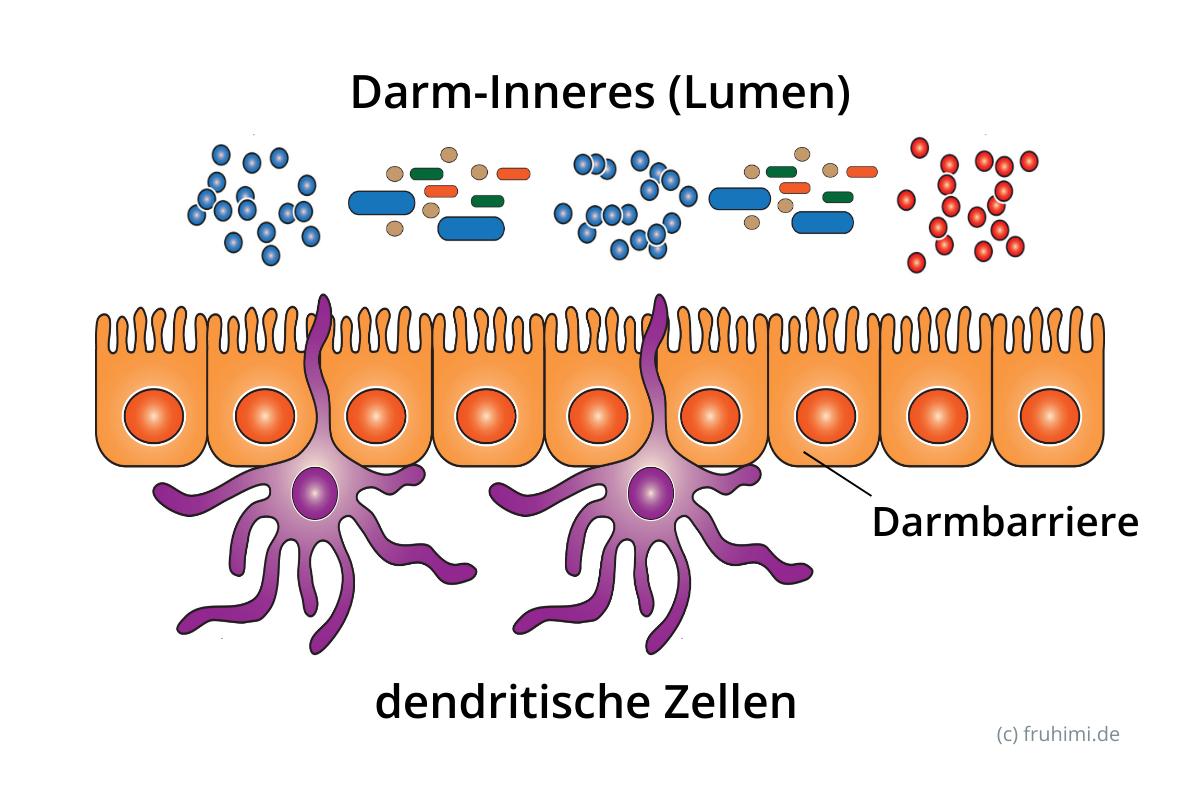
Abbildung: Dendritische Zellen dringen mit ihren langen Fortsätzen tief in das Darminnere ein und nehmen ersten Kontakt mit fremdartigen Strukturen auf. Informationen darüber geben Sie an die Lymphknoten weiter, die bei Bedarf eine Immunreaktion auslösen. / Illustration: (c) fruhimi.de. Originalbild: adobe media, Stimulation of cells vector medical illustration, von Clusterx
Antimikrobieller Schutz
Das Mikrobiom „kitzelt“ aus der Darmschleimhaut verschiedene antimikrobielle Akivitäten heraus. Die Darmbakterien liefern dem Darm mit ihren Stoffwechselprodukten und spezifischen Oberflächenstrukturen Signale, die ihn anregen, antimikrobiell aktiv zu werden. Er verstärkt daraufhin die Schleimhaut und optimiert ihre Barrierefunktion. Die Paneth Zellen der Darmschleimhaut sondern antimikrobielle Peptide und Immunglobuline ab. Diese Funktion fördern besonders Bacteroides- und Lactobacillus-Arten. Lactobacillus produziert darüber hinaus noch Milchsäure, die das Milieu ansäuert und die Zellwände anderer Bakterien knacken kann.
Das Zusammenspiel
Bacteroides-Arten regen die dendritischen Zellen der Mucosa zur Ausschüttung sekretorischer Immunglobuline an. Diese Proteine legen sich auf die Oberfläche der Bakterien und hindern sie dadurch, an die Schleimhaut anzudocken. Dadurch wird letztendlich verhindert, dass Bakterien in den Blutkreislauf übertreten.
Zudem schützt ein gesundes Mikrobiom vor dem Angriff von Pathogenen, weil die Mucosa dicht von „guten“ Bakterien besiedelt ist und den möglicherweise krankheitserregenden Bakterien den Zutritt verwehrt.
Und mithilfe der von ihnen selbst produzierten Bacteriozine („Bakterien-Gifte“) bekämpfen sich die Bakterien gegenseitig und versuchen, die anderen am Wachstum zu hindern. Fast jede Art produziert ihr eigenes Bacteriozin, das wie ein kleiner Dolch die Zellwände der Feinde aufzuschlitzen versucht.
Durch all diese Mechanismen sperrt sich auch die gute Darmflora aus. Und das ist sehr freundlich von ihr, denn auch die harmlosesten Bewohner des Darmlumen können sich in böse Pathogene verwandeln, sobald sie die Darmbarriere überwunden haben.
Veränderungen im Mikrobiom
Unser Mikrobiom ist keine statische Angelegenheit. Es ändert sich dynamisch durch viele Faktoren. Dazu zählen Alter, Ernährung und mögliche Störfaktoren wie eine Antibiotikabehandlung oder Medikamenten-Einnahme. Wenn sich die Bakteriengemeinschaft so stark verändert, dass das Mikrobiom seine Funktion nicht mehr ausüben kann, spricht man von einer Dysbiose.
Kahlschlag durch Antibiotika
Eine der wichtigsten Aufgaben eines gesunden Mikrobioms ist der Schutz vor Besiedlung durch Krankheitserreger. Aber jedes Mal, wenn wir Antibiotika einnehmen, zerstören wir damit auch den gesunden Bakterienrasen und setzen das entstandene „Brachland“ der Gefahr einer Besiedlung durch schädliche Bakterien aus. Ein Kollateralschaden, den wir gedankenlos in Kauf nehmen.
Seit langem wissen wir, dass durch die Einnahme von Antibiotika der Mechanismus, aufgrund dessen die guten Darmbakterien eine Besiedlung durch Schädlinge verhindern, gestört werden kann. Oft ist dann eine Infektion mit Salmonella typhimurium oder Clostridium difficile die Folge. Die Ursache könnte eine Störung des Netzwerkes sein, in dem die Bakterien interagieren. Eine Folge davon ist Anreicherung von Sialinsäure, die vom Wirt freigesetzt wird und das Wachstum der pathogenen Bakterien fördert. Sialinsäure ist ein natürlicher Baustein der Glycoproteine der Schleimhaut, die sonst auch den guten Darmbakterien als Nahrung dient.
Langzeitfolgen von Antibiotika
Die wesentlichen Veränderungen des Mikrobioms, die eine Antibiotikabehandlung mit sich bringt, sind der Rückgang der Artenvielfalt. Die Wiederansiedlung nützlicher Bakterienarten kann bei manchen Patienten Jahre in Anspruch nehmen, selbst nach einer Antibiotikabehandlung von nur wenigen Tagen. Auch die Artenvielfalt wird von Behandlung zu Behandlung geringer. Vor allem Aktinobakterien und Bacteroides-Arten fällt es schwer sich wieder anzusiedeln.
Ein weiteres Problem, das der Einsatz von Antibiotika mit sich bringt, ist der horizontale Gentransfer, mit dem Resistenzgene zwischen verschiedenen Individuen übertragen werden. Unser Mikrobiom ist in dieser Hinsicht sehr hilfsbereit und mitteilungsbedürftig, so dass mögliche Resistenzen sich schnell verbreiten können. In der Folge entstehen also Resistenzen gegenüber Antibiotika, wodurch spätere Behandlungen schwerwiegender Erkrankungen nicht mehr möglich sind.
Mikrobiom und Lebensalter
Das frühkindliche Mikrobiom entwickelt sich während der ersten drei Lebensjahre und entspricht ab einem Alter von etwa drei Jahren dem eines Erwachsenen. Über die weiteren Lebensdekaden bleibt das Mikrobiom weitgehend stabil. Allerdings zeigen Studien, dass bei Jugendlichen die relativen Anteile von Bacteroides und Bifidobacterium stark von denen eines erwachsenen Mikrobioms abweichen können.
Mit zunehmenden Alter verschiebt sich die Zusammensetzung der Bakteriengemeinschaft nur wenig. E. coli, Proteobakterien und Staphylokokken nehmen etwas zu und verdrängen Bifidobakterien und Firmicutes. Das kann sich in einem Rückgang der „normalen“ bakteriellen Leistungen äußern.
Ernährungseinfluss auf das Mikrobiom
Die Ernährung hat einen wesentlichen Einfluss auf die Zusammensetzung des Mikrobioms. Natürlich fängt es in frühester Kindheit an: Das Mikrobiom von Flaschenkindern unterscheidet sich von dem gestillter Säuglinge. Wir verwenden Babynahrung gedankenlos als Alternative zur Muttermilch und vergessen dabei ganz, was sie eigentlich ist: Ein Ersatz, der das Kind vor dem Verhungern schützen sollte. Sonst nichts.
Im Gegensatz dazu erfüllt Muttermilch alle Ansprüche an die Ernährung und Versorgung des Säuglings. Viele Bestandteile der Muttermilch fördern die Entwicklung eines gesunden Mikrobioms. Unverdauliche Oligosaccharide (HMO, human milk oligosaccharides) in der Muttermilch fördern gezielt das Wachstum von Bifidobacterium, das die HMOs zu den so wertvollen kurzkettigen Fettsäuren abbaut. Sie stärken auch das Immunsystem, indem sie die Ausschüttung des Immunglobulins IgG fördern. Im Mikrobiom von Flaschenkindern kommen dagegen häufiger Bacteroides und Clostridium vor. Auch im weiteren Lebensverlauf übt die Ernährung einen entscheidenden Einfluss auf die Zusammensetzung und Artenvielfalt des Mikrobioms aus.
Der Verzehr von Obst, Gemüse und ballaststoffreicher Nahrung führt generell zu einer größeren Artenvielfalt des Mikrobioms. Vor allem Vertreter der Firmicutes, die Ballaststoffe abbauen und verwerten können, kommen hier oft vor.
Wer sich hauptsächlich von unverarbeiteten landwirtschaftlichen Produkten ernährt, besitzt vermehrt Prevotella in seinem Mikrobiom, bei typischer westlicher Ernährung mit einem hohen Anteil an tierischem Eiweiß, Zucker und Stärke aber wenig Ballaststoffen gedeiht dagegen Bacteroides sehr gut.
Verschiedene Studien zeigen, dass sich das Mikrobiom in Abhängigkeit von geographischen oder klimatischen Bedingungen deutlich unterscheidet. Alle Unterschiede lassen sich aber letztendlich auf die Ernährung zurückführen, die in den entsprechenden Zonen vorherrscht (Beispiel „Mittelmeerdiät“).
Die Dysbiose des Darms
Obwohl die individuelle Zusammensetzung des Mikrobioms sehr variabel ist, liegen die verschiedenen Bakterien in einem gesunden Darm in einem harmonischen Gleichgewicht vor. Diesen Zustand bezeichnet man als Eubiose.
Eine Dysbiose dagegen ist Fehlbesiedelung des Darmes: Nützliche Bakterien werden zurückgedrängt und der Schutz vor krankmachenden, pathogenen Bakterien schwindet. Das erleichtert dann auch Fäulnisbakterien, Hefen, Schimmelpilzen und pathogenen Formen von Escherichia coli die Ansiedlung im Darm.
Folgen einer Dysbiose
 Fehlen die guten Bakterien, kann die Darmbarriere geschwächt werden und Bestandteile der Oberflächen der Bakterien ins Blut gelangen. Man spricht von einem „Leaky Gut“. Als Folge können sich stille Entzündungen im ganzen Körper ausbreiten und das Risiko für so genannte Zivilisationserkrankungen wie Diabetes mellitus Typ 2, oder Herz-Kreislauf-Erkrankungen erhöhen. Auch die Darmwand selbst kann sich entzünden. Solche Entzündungszellen gelten als die Ursache von chronisch entzündlichen Darmerkrankungen wie Morbus Crohn oder Colitis ulcerosa.
Fehlen die guten Bakterien, kann die Darmbarriere geschwächt werden und Bestandteile der Oberflächen der Bakterien ins Blut gelangen. Man spricht von einem „Leaky Gut“. Als Folge können sich stille Entzündungen im ganzen Körper ausbreiten und das Risiko für so genannte Zivilisationserkrankungen wie Diabetes mellitus Typ 2, oder Herz-Kreislauf-Erkrankungen erhöhen. Auch die Darmwand selbst kann sich entzünden. Solche Entzündungszellen gelten als die Ursache von chronisch entzündlichen Darmerkrankungen wie Morbus Crohn oder Colitis ulcerosa.
Die Darmflora nimmt auch eine wichtige Rolle in der Regulation der Immunabwehr ein. Die Bakterien nehmen Einfluss darauf, welche Strukturen als gefährlich oder harmlos eingestuft werden. Und damit auch, ob und wann eine Immunantwort ausgelöst wird. Geschehen hier Fehler, kann das Immunsystem erblinden, was vermehrte Infektionen für den Wirt bedeutet. Oder es reagiert übereifrig und greift auch harmlose Passanten an, was die Ursache von Allergien und Lebensmittel-Unverträglichkeiten sein kann.
Mittlerweile gibt es eine lange Liste von Krankheiten, die irgendwie mit dem Gesundheitszustand des Mikrobioms in Verbindung gebracht werden. Dabei sind fast alle Organsysteme betroffen. Es scheint kaum eine Krankheit zu geben, die nicht irgendwie mit der Bakteriengesellschaft in unserem Darm in Zusammenhang gebracht werden kann.
Wie äußert sich eine Dysbiose?
Die Symptome der Dysbiose haben oft direkt mit dem Verdauungstrakt zu tun. Bei
- Bauchschmerzen
- Blähungen
- Übelkeit
- Durchfall
- Lactoseintoleranz
verdächtigt man schnell den Verdauungstrakt als Ursache. Aber auch diffuse Symptome wie
- allgemeine Schwäche und
- Koordinationsstörungen sowie
- Muskel- Gelenk- und Kopfschmerzen
können auf eine Dysbiose zurückzuführen sein.
Dann gibt es wie bereits erwähnt die lange Liste von Krankheiten, die ihren Ursprung ebenfalls im Darm nehmen können und denen eine Dysbiose zu Grunde liegt, auch wenn keine der oben genannten Symptome auftreten.
Praxis: Maßnahmen für ein gesundes Mikrobiom
Probiotika: Schlüssel zu einer widerstandsfähigen Darmflora
Aufbau der Darmflora
Probiotika sind lebende Mikroorganismen, die wir unserem Körper, genauer unserem Darm, zuführen, um in den Genuss ihrer physiologischen Aktivität zu kommen. Auf Probiotika richtet sich seit einigen Jahren der Fokus der Wissenschaft, denn wenn unsere Darmbakterien uns so viel gutes tun – was läge da näher, als die erwünschten Mikroorganismen direkt dort anzusiedeln wo wir sie haben wollen?
Herausforderungen beim Einsatz von Probiotika
Experten sehen sowohl Chancen als auch Schwierigkeiten im Einsatz von Probiotika. Denn unser Darm ist ein anaerober, sauerstofffreier Lebensraum und die meisten unserer Darmbewohner sind anaerobe Bakterien, für die Sauerstoff hochgiftig ist. Sie würden den Weg vom Mund in den Darm niemals überleben und scheiden damit als Probiotikum von vornherein aus, es sei denn, sie überstehen die saure Magenpassage in einer Kapsel, die sich erst im Darm auflöst. Ein weiteres Problem ist, dass man viele der Darmbakterien nicht kultivieren kann. Das macht die massenhafte Vermehrung, die es zum Einsatz als Präbiotikum bräuchte, sehr schwierig. In anderen Fällen schienen Probiotika sich nicht dauerhaft im Darm ansiedeln zu können. Das bedeutet, dass man Probiotika dauerhaft oder zumindest langfristig einnehmen muss, um in den Genuss ihrer gesundheitsfördernden Wirkung zu kommen.
Bisher wurden weit über 1000 verschiedene Bakterienarten im Mikrobiom des Darmes gefunden. Jedes individuelle Mikrobiom enthält aber nur weniger als 200 verschiedene Arten. Was wäre, wenn man eine Art einführt, die in einem fremden, unpassenden Mikrobiom plötzlich großen Schaden anrichtet? Auch zwischen den verschiedenen Bakterien des Mikrobioms bestehen freundliche und feindliche Beziehungen.
Bei aller Vorsicht darf man aber nicht vergessen, dass zahlreiche Studien die positive Wirkung von Probiotika gegen verschiedene mit dem Mikrobiom assoziierte Erkrankungen, wie etwa Angststörungen oder das Reizdarmsyndrom, zweifelhaft nachgewiesen haben.
Welche Bakterien sind geeignet und kommen als Probiotika zum Einsatz?
Es ist nicht möglich – und auch nicht wünschenswert- irgendwelche beliebigen Bakterien als Probiotika einzusetzen. Für eine unkomplizierte Handhabe muss das Bakterium aerotolerant sein und eine Chance haben, den Magen lebend zu passieren. Und natürlich muss man sich von ihnen eine positive Wirkung auf die Gesundheit versprechen. Bifidobakterien und Lactobazillen erfüllen diese Voraussetzung.
Sie sind die am häufigsten als Probiotika eingesetzten Bakteriengattungen. Bifidobakterien produzieren kurzkettige Fettäuren, die sich im Verdauungstrakt positiv auswirken. Sie regen die Motilität des Darmes an und wirken entzündungshemmend.
Auf der Zelloberfäche von Bifidobakterien und Lactobazillen gibt es dünne, filamentöse, Haaren nicht unähnliche Strukturen, die sogenannten Pili oder auch Fimbrien. Mit ihrer Hilfe können die Bakterien sich an die Endothelzellen der Darmschleimhaut anheften. Erst dadurch wird eine dauerhafte Besiedelung des Darmes möglich. Auf diese Weise können pathogene (krankmachende) Keime von der Darmschleimhaut verdrängt werden. Sie verfügen auch über weitere, typische Zellwandstrukturen wie Lipoteichonsäure oder Peptidoglykan, die sich positiv auf die Funktion der Darmbarriere auswirken.
Vorkommen von Probiotika in Lebensmitteln
Probiotika kommen „in freier Wildbahn“ in natürlich vergorenen Lebensmitteln vor. Sauermilchprodukte wie Joghurt oder Kefir sind gute Quellen. Auch milchsauer vergorenes Gemüse wie Sauerkraut oder Kimchi oder Getränke, die aus Bio-Vollkorngetreide hergestellt werden. Der Haken an der Sache ist allerdings, dass diese Lebensmittel, wenn sie aus industrieller Produktion stammen, keine lebenden Bakterien mehr enthalten, weil sie konserviert wurden. Man muss da tatsächlich seine eigenen Kulturen pflegen.
Seit einigen Jahren bietet der Einzelhandel auch probiotische Lebensmittel an. Hierbei werden oftmals industriell hergestellten Lebensmitteln künstlich lebende Bakterien zugesetzt. Oft wird diesen Produkten auch noch eine Portion Präbiotika zugesetzt, um die Erfolgschancen der Keime zu verbessern. Diese kombinierten Produkte bezeichnet man auch als Synbiotika.
Durch den Verzehr von probiotischen Lebensmitteln kann man seinen allgemeinen Gesundheitszustand verbessern oder erhalten. Wenn sich allerdings bereits mikrobiomasssoziierte Erkrankungen anbahnen, hilft dieser sehr allgemeine Ansatz nicht mehr. Dann kommen probiotische Präparate zum Einsatz, die gezielt gegen die Beschwerden vorgehen sollen. Dabei ist es hilfreich, das richtige Probiotikum auszuwählen, denn jede Spezies, sogar jeder Stamm hat eigene, ganz individuelle Eigenschaften die zum Teil gegen verschiedene Symptome derselben Krankheit eingesetzt werden.

Bild: Fermentiertes Gemüse in Gläsern. Milchsauer vergorenes Gemüse aus eigener Herstellung besitzt einen hohen Gehalt an probiotischen Bakterien und eignet sich hervorragend zur gesunden Ernährung auf natürlicher Basis. Fotonachweis: (c) adobe media, Fermented vegetables in jars, von bit24
Präbiotika: Futter für gute Bakterien
Ist das Gleichgewicht des Darms aus dem Takt geraten, kann eine Nahrungsumstellung bei Erwachsenen innerhalb weniger Tagen zu messbaren Veränderungen des Mikrobioms führen. Diese sind reversibel – in die eine oder andere Richtung. Das bedeutet, dass es nicht ausreicht, seine Bakterien ein paar Tage zu füttern und dann wieder zur ungesunden Ernährungsweise zurückzukehren. Damit das Mikrobiom seine Leistung voll entfalten kann, muss man es dauerhaft mit dem richtigen Futter versorgen.
Was bedeutet Präbiotika bzw. Präbiotikum?
Präbiotika sind unverdauliche Nahrungsbestandteile, die gezielt das Wachstum gesundheitsfördernder Bakterien im Dickdarm fördern. Das ist der wichtige Punkt: Präbiotika können nur von bestimmten gesundheitsförderlichen Arten verwertet werden. Dadurch verschafft man ihnen einen Wachstumsvorteil und sie können sich im Mikrobiom anreichern.
Meist handelt es sich bei Präbiotika um Kohlenhydrate. Per Definition sind sie Polymere, die aus mindestens drei Zuckeruntereinheiten aufgebaut sind. Die Moleküle unterschieden sich in ihrer Komplexität, der Anzahl der Untereinheiten und dem Verzweigungsgrad. Manche sind wasserlöslich und/oder viskos. Und all diese Faktoren haben einen Einfluss darauf, ob und von welchen Darmbakterien sie fermentiert werden können. Je komplexer ein Polysaccharid ist, um so mehr verschiedene Enzyme sind nötig um es abzubauen. Ein vielfältiges Angebot an verschiedenen Ballaststoffen fördert daher die Artenvielfalt im Darm.
- Resistente Stärke
Eigentlich ist Stärke ja ein sehr gängiges Kohlenhydrat, das wir prima verdauen können. Kühlt Stärke nach dem Garen aber ab, verwandelt ein Teil davon sich sich in so genannte resistente Stärke, die von unseren Verdauungsenzymen nicht mehr gespalten werden kann. So kann sie es in den Dickdarm schaffen und dort die Bakterien füttern.
- Beta-Glucane
Bei Beta-Glucanen handelt es sich um lösliche Ballaststoffe, die in den Zellwänden von Getreide oder Pilzen vorkommen. Vor allem Hafer und Gerste sind reich an Beta-Glucanen. In unserer Ernährung ist nur Hafer eine nennenswerte Quelle für Beta-Glucane, wobei man auf Vollkornprodukte oder Kleie zurückreifen sollte, denn die Ballaststoffe befinden sich hauptsächlich in den Randschichten der Körner. Haferkleie enthält etwa acht Prozent Beta-Glucan.
- Inulin
Inulin ist ein Gemisch von verschieden langen Polysacchariden, die aus Fructose aufgebaut sind. Pflanzen produzieren Inulin als Reservestoff. Es kommt reichlich in den Wurzelknollen von Korbblütlern vor. Topinambur, Chicorée, Schwarzwurzel, Pastinaken, Löwenzahn und Artischocken sind gute Quellen.
- Fructo-Oligosaccharide (FOS)
Fructo-Oligosaccharide bestehen aus einem Molekül Saccharose, dem noch ein bis drei Fructose-Moleküle anhängen. FOS kommen in Bier, Bananen, Roggen und Hafer, Tomaten, Spargel, Knoblauch und Zwiebeln vor.
- Lactulose
Lactulose entsteht beim Erhitzen oder Lagern von Milch. Es besteht aus einem Galactose- und einem Fructose-Molekül. Sie wird von den Darmbakterien zu Lactat und Pyruvat vergoren und fördert das Wachstum von Bifidobakterien.
- Galacto-Oligosaccharide (GOS)
Galacto-Oligosaccharide bestehen aus bis zu sieben Galactose-Einheiten und einem Glucoserest. Sie sind ein wesentlicher Bestandteil von Muttermilch und fördern das Wachstum von Bifidobakterien. In Kuhmilch sind sie nicht enthalten.
- Pektin
Pektine sind pflanzliche Polysaccharide, die aus Polyuroniden aufgebaut sind. Sie kommen unter anderem reichlich in Hagebutten, Äpfeln, Aprikosen, Karotten oder Citrusschalen vor.
Stuhltransplantation als Mittel zur Darmsanierung
Wenn herkömmliche Massnahmen nicht mehr helfen, die Fehlbesiedelung des Darmes zu korrigieren, kann eine Stuhltransplantation Abhilfe schaffen. Eine Stuhltransplantation oder Fäkale Mikrobiota-Transplantation (FMT) ist die Übertragung von Stuhl (oder den daraus gewonnenen Bakterien) eines gesunden Spenders auf einen Empfänger, dessen Mikrobiom irreparabel gestört ist.
Als Spender werden bevorzugt Personen aus dem persönlichen Umfeld des Patienten gewählt, weil man davon ausgeht, dass ihre Mikrobiome sich ähneln und die Gefahr von Infektionen durch all zu fremde Bakterien möglichst gering ist.
Der Spenderstuhl wird mit physiologischer Kochsalzlösung vermischt, grob gefiltert und die Suspension durch einen Einlauf in den Dickdarm oder eine Duodenalsonde in den Zwölffingerdarm gespritzt. Die Methode wird oft erfolgreich gegen Infektionen mit Clostridium difficile angewandt.
Mikrobiom-assoziierte Krankheiten
Mikrobiom und chronisch entzündliche Darmerkrankungen (CED)
Als chronisch entzündliche Darmerkrankungen bezeichnet man die beiden Krankheiten Morbus Crohn und Colitis ulcerosa.
Colitis ulcerosa ist eine Entzündung die ausschließlich die Darmschleimhaut im Bereich des Dickdarms betrifft. Als Symptome können wiederkehrender Durchfall, Koliken und Darmblutungen auftreten.
Morbus Crohn dagegen ist eine chronische Entzündung des Darmes, von der neben der Darmschleimhaut auch tiefere Gewebsschichten betroffen sind. Die Entzündungen treten meist am unteren Ende des Dünndarms und oberen Ende des Dickdarms auf, grundsätzlich kann aber der gesamte Magen-Darm-Trakt betroffen sein. Die typischen Symptome sind Bauchschmerzen und anhaltender Durchfall.
Pathogenese der CED
Beiden Erkrankungen liegt eine Entzündung der Darmschleimhaut zugrunde. Das grundlegende Problem scheint zu sein, dass das Immunsystem des Darmes nicht mehr zwischen Freund und Feind unterscheiden kann. Als Folge kommt es zu einer krankhaft gesteigerten Immunreaktion gegen die Darmbakterien. Möglicherweise liegt eine genetische Prädisposition vor, denn bei CED Patienten findet man vermehrt eine Mutation im so genannten NOD2 Gen.
Das NOD2 Gen codiert für ein Protein, das bestimmte Bestandteile der Bakterienwand, die Lipopolysaccharide, erkennt. Bei Trägern des mutierten und dadurch verkürzten Gens versagt hier die angeborene Immunabwehr. Die erworbene Immunabwehr löst bei einer wiederkehrenden Infektion dann eine heftige Reaktion aus, die zu einer übermäßig starken Produktion von Abwehrmolekülen führt, die dann zu den typischen Entzündungsreaktionen führt.
Es ist möglich, dass das Immunsystem von CED Patienten das Mikrobiom sehr effektiv bekämpft, denn bei CED Patienten sind tatsächlich 25% weniger Gene im Darm nachweisbar, was auf eine reduzierte Artenvielfalt schließen lässt. Insgesamt sind die Veränderungen des Mikrobioms aber eher Folge als Ursache der Erkrankung.
Die Rolle des Mikrobioms bei Reizdarm (RDS)
Pathogenese des Reizdarmsyndroms
Ein Reizdarm beruht auf einer funktionellen Störung des Darms. Typische Symptome sind Bauchschmerzen, Blähungen und Durchfall oder Verstopfung. Es ist bisher nicht vollkommen verstanden, wie ein Reizdarm entsteht, aber es finden Veränderungen im Darm statt, die denen bei chronisch entzündlichen Darmerkrankungen ähneln.
 Symptome können auch durch eine erhöhte Durchlässigkeit der Darmschleimhaut ausgelöst werden. Gewebeproben aus der Darmschleimhaut betroffener Menschen zeigen eine erhöhte Immunaktivität. Mitunter ist ein Reizdarm die Folge eines Magen-Darm-Infektes, vor allem durch Campylobacter jejuni. Nach aktuellem Kenntnisstand ist ein Ungleichgewicht im Darmmikrobiom ein Faktor, der die Entstehung eines Reizdarms begünstigt.
Symptome können auch durch eine erhöhte Durchlässigkeit der Darmschleimhaut ausgelöst werden. Gewebeproben aus der Darmschleimhaut betroffener Menschen zeigen eine erhöhte Immunaktivität. Mitunter ist ein Reizdarm die Folge eines Magen-Darm-Infektes, vor allem durch Campylobacter jejuni. Nach aktuellem Kenntnisstand ist ein Ungleichgewicht im Darmmikrobiom ein Faktor, der die Entstehung eines Reizdarms begünstigt.
Man vermutet außerdem, dass beim Reizdarmsyndrom die Motilität des Darmes gestört ist. Die Peristaltik wird durch das enterische Nervensystem gesteuert und zum Teil durch das Mikrobiom aktiviert. Störungen im Serotoninhaushalt könnten die Schmerzwahrnehmung dahingehend verändern, dass man seinen Darm einfach intensiver spürt.
Obwohl der Zusammenhang zwischen einem Reizdarm und einer Dünndarmfehlbesiedelung noch kontrovers diskutiert wird, sehen viele Experten eine Fehlbesiedelung des Dünndarms (DDFB oder SIDO für small intestine bacterial overgrowth) als Hauptursache für das Reizdarmsyndrom.
Andere sehen es genau umgekehrt und verdächtigen den strapazierten Darm, die Fehlbesiedelung des Dünndarms erst zu ermöglichen. Fakt ist jedenfalls, dass beide Krankheitsbilder in vielen Fällen überlappen.
Dünndarmfehlbesiedelung (SIBO) und Mikrobiom
Jeder Darmabschnitt hat seine eigenen, dort typischerweise ansässigen Bakterien. Von einer Dünndarmfehlbesiedelung spricht man, wenn der Dünndarm mit Bakterien, die dort eigentlich gar nicht hingehören, besiedelt ist. Meist stammen die Einwanderer aus dem Dickdarm, sie kommen also aus umgekehrter Richtung aus dem Darmende.
Small intestine bacterial overgrowth (SIBO)
Von SIBO spricht man ab einer Populationsdichte von 10 hoch 5 (100.000) bis 10 hoch 6 (1.000.000) Bakterien pro Milliliter Darmvolumen. Normalerweise gibt es im Dünndarm nur maximal 10³ (1.000) Bakterien pro Milliliter. Die Bakterien aus dem Dickdarm vergären die im Dünndarm noch reichlich vorhandenen Nährstoffe. Dabei entstehen Gase, die einen Blähbauch verursachen können. Ein Teil der Gase geht ins Blut über und wird mit der Atemluft abgegeben, so dass man sie in einem typischen Atemtest nachweisen kann. Der größte Teil des Gases verbleibt aber im Darm, dehnt die Darmwand und verursacht die typischen Schmerzen.
Die Ursachen, die zu einer Fehlbesiedlung des Dünndarms führen können, sind vielfältig. Anatomische Anomalien kommen infrage, ebenso wie Krankheiten, die die Motilität des Darmes herabsetzen, sowie viele weitere Faktoren.
Behandlung einer Dünndarmfehlbesiedelung
Die klassische Behandlung einer Dünndarmfehlbesiedlung besteht meist aus einer Antibiotikatherapie mit Rifaximin. Dieses Medikament ist ausschließlich im Darm wirksam und wird vom Körper kaum aufgenommen.
Pflanzliche Präparate zeigen nach neueren Studien eine ebenso gute Wirksamkeit wie Rifaximin. Das wurde für Pfefferminzöl, Allicin (aus Knoblauch), Neemöl, Sauerdornbitter (Berberine), Oregano und Wermut gezeigt. Unterstützend können noch Pro- und Präbiotika zum Einsatz kommen.
Mikrobiom bei pseudomembranöser Colitis
Pseudomembranöse Colitis ist eine Entzündung des Dickdarmes, die durch die Einnahme von Antibiotika ausgelöst wird. Dadurch werden große Teile der residenten Darmflora abgetötet und resistente Keime, darunter Clostridium difficile, vermehren sich übermäßig. Diese Bakterien produzieren Toxine, die der Auslöser der Entzündung sind. Es führt zu Verlusten von Flüssigkeit, Proteinen und Chlorid und hemmt die Resorption von Glucose, Natrium und Aminosäuren. Heftige Durchfälle sind die Folge.
Das Mikrobiom bei Übergewicht und Fettleibigkeit
Das Mikrobiom beeinflusst unter anderem auch unser Körpergewicht. Kann es sein, dass manche Bakterien dick und andere dünn machen?
Bacteroidetes und Firmicutes machen den Bärenanteil unseres Mikrobioms aus. Neunzig Prozent unserer Darmbakterien gehören einer dieser Gruppe an, wobei allerdings zu jeder Gruppe unzählig viele verschiedene Arten gehören.
Nun findet man im Mikrobiom von schlanken und übergewichtigen Menschen unterschiedliche Bakterien vor. Bei schlanken Menschen findet man überwiegend Bakterien der Bacteroidetes Gruppe während bei Übergewichtigen die Firmicutes dominieren. Eine solche Verschiebung der Zusammensetzung des Mikrobioms wirkt sich direkt auf den Energiestoffwechsel der Betroffenen aus. Das konnten Studien zeigen, bei denen keimfreie Mäuse bei identischer Fütterung weniger an Gewicht zunahmen, als ihre Artgenossen mit einem gesunden Mikrobiom.
Überträgt man das Mikrobiom von genetisch identischen Mäusen, die sich nur in Bezug auf ihr Körpergewicht unterscheiden, in die Verdauungskanäle steriler Mäuse, dann nehmen diejenigen mehr an Gewicht zu, welche die Bakterien der dicken Mäuse erhalten haben. Und das auch, wenn sie fettarme, ballaststoffreiche Kost erhalten.
Das zeigt deutlich, dass ein verändertes Mikrobiom eine Ursache der Fettleibigkeit ist und sich nicht als Folge eines Überkonsums an Nahrung verändert.
Bakterien erhöhen den verfügbaren Energiegehalt der Nahrung
Die Darmbakterien fettleibiger Menschen produzieren deutlich mehr Enzyme, mit deren Hilfe sie Ballaststoffe wie Zellulose zu leicht verdaulichen Einfachzuckern abbauen können. So erhöht sich der für den Wirt verfügbare Energiegehalt der Nahrung deutlich und eine Stange Sellerie kann so stark zu Buche schlagen wie ein Schokoriegel. Oft entschuldigen Übergewichtige sich mit dem Hinweis, dass die Gene schuld an ihrem Zustand seien. Und sie haben recht. Nur sind es nicht die eigenen Gene. Das ist gut, denn die eigenen Gene kann man nicht verändern. Die symbiontischen Gene aus dem Mikrobiom aber schon.
Angehörige der Firmicutes sind wichtig für den Spaltung und Fermentation pflanzlicher Ballaststoffe. Sie bauen diese zu kurzkettigen Fettsäuren, wie Butyrat oder Propionat ab. Diese Stoffwechelsprodukte stehen dann dem Wirt zur Emergiegewinnung zur Verfügung. Sie dienen im Dickdarm, die Zellen der Schleimhaut zu ernähren. Aber sie steuern auch in einem ausgewogenen Mikrobiom bis zu zehn Prozent der Gesamtenergie zur Nahrung bei. Sind Firmicutes deutlich in der Überzahl, bringen die Träger in der Regel ein höheres Körpergewicht auf die Waage.
Firmicutes sind eine bunte Truppe und lassen sich in viele weitere Gattungen wie Ruminococcus, Lactobacillus, Faecalibacterium oder Roseburia unterteilen. Auch Clostridium ramosum zählt zu den Firmicutes und steht unter Verdacht Übergewicht zu fördern. C. ramosum gedeiht besonders gut bei fettreicher Ernährung und fördert die Bildung so genannter enterochromaffiner Zellen. Diese spezialisierten Zellen produzieren den Botenstoff Serotonin und der wiederum veranlasst die Bildung von Fettsäuretransportern. Dadurch können Nahrungsfette besser resorbiert werden und zur Entstehung von Übergewicht beitragen.
In jüngster Zeit kristallisiert sich allerdings heraus, dass möglicherweise doch die eigenen Gene ein bisschen schuld sind, wenn man ein paar Pfunde zu viel mit sich herumträgt. Das Darmbakterium Christensenella, das zur Gruppe der Clostridien gehört, scheint einen positiven Effekt auf die schlanke Linie zu haben. Wie es das macht ist bisher aber ein Rätsel, aber schlanke Menschen haben deutlich mehr davon im Darm. Und sein Präsenz im Darm scheint auch von humangenetischen Faktoren abzuhängen.
Unter den Bacteroidetes dominieren die Gattungen Bacteroides und Prevotella. Bacteroides ist vor allem in die Verarbeitung stärkehaltiger Nahrungsmittel involviert, während Prevotella bei unverarbeiteter Nahrung dominiert. Mehrere Studien konnten zeigen, dass Prevotella am Gewichtsverlust nach einer Nahrungsumstellung auf mediterrane Kost beteiligt ist.
Eine weitere Gattung der Bacteroidetes ist Alistipes. Sie steht in Zusammenhang mit einer fleischreichen und kalorienreichen Ernährung. Alistipesarten werden einerseits mit einem Schutz vor bestimmten Erkrankungen wie Leberzirrhose oder kardiovaskulären Erkrankungen in Verbindung gebracht. Andererseits erscheinen sie in anderen Studien als Risikofaktor für Darmkrebs oder psychische Erkrankungen.
Abnehmen und Übergewicht
Überwiegt Prevotella, dann fällt das Abnehmen leicht und die „Pfunde purzeln“ bei getreidereicher Kost. Ist Bacteroides die vorherrschende Bakterienart, so kann man mit dieser Kost wenig Erfolge erzielen. Stattdessen führen hier inulinreiche Ernährungsformen, die die Vermehrung von Bacteroides und Bifidobakterien fördern, zum Erfolg.
Während also das generelle Verhältnis zwischen Bacteroidetes und Firmicutes ein Indikator für Übergewicht ist, gibt das Verhältnis zwischen Prevotella und Bacteroides Hinweise darauf, wie schwer oder leicht man das überflüssige Gewicht wieder abbauen kann.
Akkermansia mögen kein Fett
Ein weiteres Bakterium, das gut für ein gesundes Körpergewicht ist, ist Akkermansia muciniphila. Diese Bakterien machen bei normalgewichtigen Menschen drei bis fünf Prozent der Darmflora aus, kommen bei Übergewichtigen aber viel seltener vor. Akkermansien pflegen die Mucosa und halten dadurch die Darmbarriere intakt. Warum sich das auf das Körpergewicht des Wirts auswirkt ist noch nicht klar. Möglicherweise greifen die von den Bakterien produzierten kurzkettigen Fettsäuren über verschiedene Rezeptoren in die Regulation des Sättigungsgefühls ein. Akkermansien mögen kein Fett: Eine fettreiche Ernährung hindert sie an der Vermehrung. Bei einer fettarmen und proteinreichen Ernährung gedeiht Akkermansia muciniphila dagegen sehr gut.
Diabetes und Mikrobiom
Diabetes ist eine Störung des Kohlenhydratstoffwechsels. Er beruht entweder auf einem absoluten Insulinmangel, etwa wenn die Produktion des Hormons in der Bauchspeicheldrüse versagt (Typ-1-Diabetes) oder einem relativen Insulinmangel, wenn insulinabhängige Gewebe gegenüber dem Insulinsignal erblinden (Typ-2-Diabetes). Die Folge ist ein andauernd krankhaft erhöhter Blutzuckerspiegel, der langfristig an verschiedenen Organen und Geweben erhebliche Schäden anrichten kann. Das Mikrobiom kann sowohl an der Entstehung von Typ-1 als auch an der Entstehung von Typ-2-Diabetes beteiligt sein.
Gründe für die Entstehung von Diabetes
Die Ursachen, die zur Entstehung von Typ-2-Diabetes führen sind Übergewicht, ungesunde Ernährung und Bewegungsmangel. Auch eine genetische Komponente besteht, denn die Veranlagung zu Typ-2-Diabetes tritt familiär gehäuft auf. Und in neuester Zeit mehrt sich auch der Verdacht, dass Darmabakterien die Entstehung von Typ-2-Diabetes begünstigen oder verhindern können.
Diabetes-Typ 2 beginnt mit einer Insulinresistenz der glukoseabhängigen Organe. Die Ursache dafür ist eine permanente Zufuhr von Glukose in den Blutkreislauf. Um die resistenten Gewebe doch noch zur Abnahme des Blutzuckers zu bewegen, muss die Bauchspeicheldrüse immer mehr Insulin produzieren. Auf Dauer erschöpfen sich die β-Zellen und die Insulinproduktion der Bauchspeicheldrüse kommt zum Erliegen.
Welcher Zusammenhang besteht nun zwischen Diabetes und dem Mikrobiom?
Der Zusammenhang zwischen Diabetes-Typ 2 und Mikrobiom könnte indirekt sein, denn das Mikrobiom hat einen Einfluss auf das Körpergewicht und viele Typ-2-Diabetiker sind adipös. Die Mechanismen, nach denen das Mikrobiom der Entstehung von Diabetes-Typ 2 entgegenwirkt, scheinen denen des Einflusses auf das Körpergewicht sehr ähnlich zu sein.
Kurzkettige Fettsäuren (SCFA) als Knotenpunkt
Das Mikrobiom steuert kurzkettige Fettsäuren (short-chain fatty acids: SCFA) aus der Fermentation von Ballaststoffen und Proteinen im Dickdarm zum Energiestoffwechsel des Wirts bei. SCFA sind Abfallprodukte des bakteriellen Stoffwechsels. Am häufigsten werden Acetat, Propionat und Butyrat gebildet, wobei Acetat und Propionat ein Produkt der Bacteroidetes sind während Firmicutes Butyrat produzieren.
Butyrat in der Nahrung verbessert die Insulinresistenz, vermutlich indem es den Energieverbrauch steigert und die Funktion der Mitochondrien verbessert. Erstaunlicherweise ist der Gehalt an SCFA im Stuhl übergewichtiger Menschen höher als bei schlanken. Das liegt möglicherweise daran, dass bei Fettleibigen die Resorption der SCFA in Dickdarm vermindert ist.
SCFA fungieren als Signalmoleküle, die verschiedene Stoffwechselwege aktivieren können, die den Stoffwechsel von Fett, Cholesterin und Glukose beeinflussen.
Darüber hinaus aktivieren SCFA über die Fettsäurerezeptoren FFAR2 und FFAR3 GLP-1 ein Hormon aus dem Darm, das unter anderem die Insulinausschüttung und das Sättigungsgefühl fördert. Mäuse, denen der Fettsäurerezeptor fehlt, entwickeln Übergewicht während große Mengen dieses Proteins mit einem schlanken Körper einhergehen.
Endotoxine und stille Entzündungen
Leichte Entzündungen sind ein typisches Symptom von sowohl Übergewicht als auch Typ-2-Diabetes. Entzündungsfördernde Zytokine spielen eine wichtige Rolle für immunologische Reaktionen und bei Entzündungsprozessen. Ihre Synthese wird durch bakterielle Lipopolysaccharide aktiviert. Diese Moleküle sind Bestandteile der äußeren Zellwand von vielen Bakterien.
Bei einer Schwäche der Darmbarriere können bakterielle Lipopolysaccharide vermehrt in das Blut übertreten. Sie werden dann als Endotoxine bezeichnet und können überall im Körper stille Entzündungen auslösen.
Über einen komplizierten Mechanismus können Endotoxine die Ausschüttung von Insulin aus den β-Zellen der Bauchspeicheldrüse hemmen und auch die Bauchspeicheldrüse schädigen. Die Darmbarriere wird undicht, wenn die Schleimhaut nicht intakt ist. Studien haben gezeigt, dass eine Wiederherstellung der Mukusschicht (Darmschleimhaut) durch Akkermansia muciniphila den Nüchternblutzuckerspiegel bei Diabetikern senken kann. Somit übt Akkermansia über zwei Mechanismen einen Schutz vor Diabetes aus: Es produziert kurzkettige Fettsäuren, die die Insulinsensitivität verbessern und schützt den Wirt vor Endotoxinen, die über stille Entzündungen die Entstehung von Diabetes fördern.
Autoimmunerkrankungen und Mikrobiom
Autoimmunkrankheiten sind Krankheiten, bei denen sich das Immunsystem fälschlicherweise gegen das gesunde körpereigene Gewebe richtet. Die Häufigkeit von Autoimmunkrankheiten hat in den vergangenen Jahrzehnten stark zugenommen. Die Auslöser sind nicht vollkommen verstanden, es werden Umweltreize und eine Veranlagung diskutiert. Und auch das Darmmikrobiom scheint eine tragende Rolle bei der Entstehung von Autoimmunkrankheiten zu spielen.
Studien haben gezeigt, dass Veränderungen in der Zusammensetzung des Darmmikrobioms zum Verlust der Immuntoleranz führen können. Als Folge greift das Immunsystem grund- und wahllos verschiedene Gewebe an. Patienten, die an Autoimmunkrankheiten leiden, weisen ein im Gegensatz zu Gesunden deutlich verändertes und an Arten reduziertes Darmmikrobiom auf. In ihrem Darm findet man vermehrt Enterobakterien und Fusobakterien und im Mausmodell konnte gezeigt werden, dass E.coli, Yersinia und Clostridium difficile am Entstehen von chronisch entzündlichen Darmerkrankungen beteiligt sind.
Multiple Sklerose (MS) ist eine Autoimmunkrankheit, bei der Immunzellen die isolierende Myelinschicht der Nervenzellen angreifen und dadurch zu neurologischen Ausfällen führen. Bei Betroffenen findet man einen Rückgang verschiedener Bacteroides Arten, Faecalibakterien und den Produzenten kurzkettiger Fettsäuren während vermehrt Enterobakterien und Methanobrevibacter vorkommen. Nach der Verabreichnung von Medikamenten gegen MS steigt der Anteil von Prevotella, während Clostridium perfringens daraufhin Toxine produziert, die Krankheitsschübe auslösen können.
Auch Typ-1-Diabetes ist eine Autoimmunkrankheit und zeigt charakteristische Veränderungen des Mikrobioms. Besonders auffällig sind die geringen Keimzahlen von Intestimonas, einem Butyrat produzierenden Darmbakterium, während man vermehrt Blautia findet. Diese Bakterien schützen vor der Graft-versus-Host-Reaktion, einer Komplikation, die nach Knochenmarkstransplantationen auftreten kann. Dabei richten sich Immunzellen des implantierten Gewebes gegen den Empfänger.
Auch bei rheumatoider Arthritis oder Nahrungsmittelallergien spielt das Mikrobiom über Immumfunktionen eine Rolle.
Die Rolle des Mikrobioms bei psychischen und neurologischen Erkrankungen
Dass unser Mikrobiom auf vieles, was in unserem Körper passiert, einen Einfluss ausübt, haben wir schon akzeptiert. Aber wie sieht es mit psychischen und neurologischen Krankheiten aus? Sie haben ihren Ursprung im Nervensystem – aber ist das nicht weit weg vom Darm? Nein, ist es nicht.
Das enterische Nervensystem
Zwischen dem zentralen Nervensystem und dem Magen-Darm-Trakt besteht ein enger Kontakt. Das gesamte Verdauungssystem wird vom enterischen Nervensystem, dem ENS, durchzogen. Das ist neben dem Sympathicus und Parasympathicus ein Teil des vegetativen Nervensystems und wird gerne salopp als Bauchhirn oder zweites Gehirn bezeichnet. Schon während der Embryonalentwicklung trennt sich ein Teil des Nervengewebes ab und wandert in den zukünftigen Verdauungstrakt.
Das enterische Nervensystem besteht aus einem Nervengeflecht, das zwischen der Darmwand und den umgebenden Muskelschichten liegt. Die Nervenzellen regulieren die Verdauung, steuern die Peristaltik und Darmentleerung. Damit haben wir den Kopf frei für andere Dinge, denn das Bauchhirn arbeitet vollkommen selbständig. In der Geschäftswelt nennt man das Outsourcing.
Kopf und Darmhirn stehen über den Vagusnerv in Verbindung. Der Vagusnerv ist einer der zwölf Hirnnerven und der einzige, der den Kopf verlässt und mit dem Rest des Körpers kommuniziert. Und es findet eine rege Kommunikation statt, bei der neunzig Prozent der Information vom Darm zum Kopf wandert und nur zehn Prozent im umgekehrter Richtung. Diese Verbindung bezeichnet man als Darm-Hirn-Achse.
Der Darm produziert eine Reihe von Peptidhormonen. Der Magen-Darm-Trakt ist damit in der Tat die größte endokrine Drüse der Säugetiere, die Dutzende von Signalmolekülen in Umlauf bringt. Die Peptidhormone aus dem Darm können an Rezeptoren von Immunzellen der Nervenenden des Vagusnerves andocken und dadurch in die Kommunikation zwischen Darm und Hirn eingreifen.
Depressionen und Angststörungen
Welche und wie viel Peptidhormone gebildet werden, hängt nicht zuletzt von der Zusammensetzung des Mikrobioms ab. Es zeichnet sich ab, dass die Wechselwirkungen zwischen den Darmbakterien und Peptidhormonen von großer Bedeutung sind für die Regulation der Signalübertragung zwischen Darm und Hirn. Die Darm-Hirn-Achse scheint eine wichtige Rolle bei der Entstehung psychischer Erkrankungen wie Angststörungen oder Depressionen zu spielen.
Depressionen und Angststörungen gehen oft mit einer veränderten Motilität des Darmes einher und das verändert wiederum die Zusammensetzung der Darmgesellschaft. Bewegt sich der Darm schneller, werden pro Zeiteinheit auch mehr Bakterien abgegeben und bestimmte Arten können so ausgedünnt werden. Bewegt sich der Darm langsamer, haben sie mehr Zeit, sich zu vermehren, bevor sie ausgeschieden werden und können sich anreichern. Im Tiermodell hat sich gezeigt, dass bei Depressionen der Anteil der Bacteroidetes gegenüber Firmicutes deutlich ansteigt.
Bei chronischem Stress sinkt der Anteil der Bacteroidetes dagegen, während sich Clostridien vermehren. Veränderungen der Clostridienzahlen sind im allgemeinen ein Indikator für veränderte Konzentrationen von Botenstoffen wie etwa Serotonin, dem „Glückshormon“. Interessanterweise haben Antidepressiva oft auch antibiotische Aktivität, während manche Antibiotika auch antidepressiv wirken.
Darmbakterien produzieren Metabolite
Inzwischen steht fest, dass das Mikrobiom einen Anteil an der Entstehung von Depressionen und Angststörungen hat. Die Darmbakterien produzieren Metabolite, die im Wirt als Neurotransmitter, wie Serotonin oder GABA (Gamma-Aminobuttersäure), wirken. Das Vorhandensein von Butyrat-produzierenden Bakterien im Darm, wie Koprokokken und Faecalibacterien, geht mit einer höheren Lebensqualität des Wirts einher. Koprokokken und auch Bakterien der Gattung Dialister sind bei depressiven Menschen in ihrer Anzahl reduziert.

Abbildung: Auch neurologische Erkrankungen wie Parkinson, Alzheimer, Autismus oder Schizophrenie zeigen Veränderungen des Mikrobioms. In manchen Fällen kann ein direkter Zusammenhang zwischen der Erkrankung und bestimmten Bakteriengruppen hergestellt werden. Bildnachweis: Parkinson Disease Tremor Symptoms Concept, von wladimir1804, (c) adobe media
Bakterienpopulation bei Depression und Autismus
Bei depressiven Patienten findet man eine hohe Bacteroides-Population, während Angehörige der Lachnospiraceae unterrepräsentiert sind. Bei autistischen Kindern fehlt es an Prevotella und Koprokokken im Darm.
Mikrobiom und Atherosklerose
Atherosklerose bezeichnet die krankhafte Einlagerung von Cholesterin und anderen Fetten in die innere Wandschicht der arteriellen Blutgefäße. Sie tritt bevorzugt an den Herzkranzgefäßen und der Halsschlagader auf und stellt ein erhöhtes Risiko für Herzinfarkt und Schlaganfall dar. Es handelt sich dabei um einen chronisch entzündlichen Prozess. Im Laufe der Zeit entstehen Plaques, die die Gefäße verengen, den Blutfluss behindern und die Sauerstoffversorgung gefährden.
Viele Faktoren, wie Übergewicht, Diabetes oder stille Entzündungen, an denen das Mikrobiom beteiligt sein kann, begünstigen die Entstehung einer Atherosklerose. Nun mehren sich aber Hinweise, dass auch ein direkter Zusammenhang zwischen der Zusammensetzung des Mikrobioms und der Entwicklung von Atherosklerose besteht.
Die Darmbakterien bauen nämlich Carnitin und Lecithin, die besonders reichlich in rotem Fleisch, Eiern und Meeresfrüchten enthalten sind, zu Trimethylamin (TMA) ab. Das wird in der Leber zu Trimethylamin-N-Oxid (TMAO) weiter verstoffwechselt und diese Verbindung fördert die Einlagerung von Fetten in die so genannten Schaumzellen in den Plaques.
Dieser Prozess kann sowohl durch die Gabe eines Hemmstoffes der TMAO Synthese als auch Antibiotika unterbunden werden. Das zeigt, dass de Bakterien direkt an der TMAO Synthese und damit an der Verbreitung der Plaques beteiligt sind.
Die Rolle des Mikrobioms bei der Krebsentstehung
Krebs umfasst viele verschiedene Erkrankungen, die alle gemeinsam haben, dass Körperzellen sich verändern und sich daraufhin unkontrolliert vermehren. Als Ursachen für eine Krebserkrankungen kommen verschiedene Faktoren infrage. Es kann eine genetische Prädisposition vorliegen. Schädliche Umwelteinflüsse können Mutationen auslösen, die eine Krebserkrankung nach sich ziehen. In manchen Fällen ist Krebs auch auf eine Infektion zurückzuführen, wie zum Beispiel Gebärmutterhalskrebs, der durch ein Virus, das Human Papilloma Virus (HPV) ausgelöst wird. Auch Bakterien können am Entstehen einer Krebserkrankung beteiligt sein, wie der Magenkeim Helicobacter pylori, der, ebenso wie HPV, für etwa ein Drittel der weltweit durch Infektionen ausgelösten Krebsfälle verantwortlich ist.
Nach derzeitigem Kenntnisstand sind Mikroorganismen, die nicht unbedingt Bakterien sein müssen, in etwa zwanzig Prozent der Fälle entscheidend am Entstehen einer Krebserkrankung beteiligt.
Das Mikrobiom kann guten oder schlechten Einfluss auf den Verlauf einer Krebserkrankung nehmen: Es kann das Geschehen hemmen oder vorantreiben. Es kann die Proliferation oder den Tod von Tumorzellen, zum Beispiel durch die Produktion genotoxischer Substanzen, herbeiführen. Es kann in die antitumoralen Immunfunktionen eingreifen oder Moleküle metabolisieren, die für die Krebsentstehung oder -entwicklung von Bedeutung sind. Das können Metabolite des Wirtes, Nahrungsbestandteile oder Medikamente sein.
Studien haben einen Zusammenhang zwischen dem vermehrten Auftreten von Fusobacterium nucleatum und Darmkrebs gezeigt: Im Mausmodell beschleunigt F. nucleatum das Wachstum des Tumors. Das Bakterium produziert auch ein Protein namens Fap2, welches auf einigen T-Zellen und natürlichen Killerzellen vorkommt, und schaltet so die natürliche Immunüberwachung aus. Eine gestörte Darmbarriere kann entzündungsfördernd wirken und die Entstehung einer Krebserkrankung begünstigen. Durch eine gestörte Darmbarriere können Bakterientoxine in den Körper gelangen, die auch in anderen Organen Krebs entstehen lassen.
Nicht immer sind es einzelne Mikroorganismen, die Einfluss auf die Krebserkrankung nehmen. In manchen Fällen scheint die individuelle Zusammensetzung des Mikrobioms eine wesentliche Rolle zu spielen. Im Fall von Darmkrebs findet man neben F. nucleatum eine Reihe weiterer Indikatorbakterien, die mit dem Auftreten der Krankheit assoziiert werden.
Allerdings können Darmbakterien bei einer Krebserkrankung auch gesundheitsfördernd wirken oder die Therapie unterstützen. Aktuelle Studien zeigen, dass der Erfolg einer Krebstherapie bei Lungenkrebs oder schwarzem Hautkrebs von der Anwesenheit von Bifidobakterium im Darm abhängt.
Quellenangaben:
Jandhyala, Sai Manasa et al. “Role of the normal gut microbiota.” World journal of gastroenterology vol. 21,29 (2015): 8787-803. doi:10.3748/wjg.v21.i29.8787
Maier, Lisa et al. “Extensive impact of non-antibiotic drugs on human gut bacteria.” Nature vol. 555,7698 (2018): 623-628. doi:10.1038/nature25979
Woting A, et al. Clostridium ramosum Promotes High-Fat Diet-Induced Obesity in Gnotobiotic Mouse ModelsmBio 2014 Sep 30;5(5):e01530-14. doi: 10.1128/mBio.01530-14.
Goodrich J, et al. Human genetics shape the gut microbiome 2014 Nov 6;159(4):789-99. doi: 10.1016/j.cell.2014.09.053.
Parker, Bianca J et al. “The Genus Alistipes: Gut Bacteria With Emerging Implications to Inflammation, Cancer, and Mental Health.” Frontiers in immunology vol. 11 906. 9 Jun. 2020, doi:10.3389/fimmu.2020.00906
Geerlings, Sharon Y et al. “Akkermansia muciniphila in the Human Gastrointestinal Tract: When, Where, and How?.” Microorganisms vol. 6,3 75. 23 Jul. 2018, doi:10.3390/microorganisms6030075
Clark, Allison, and Núria Mach. “Exercise-induced stress behavior, gut-microbiota-brain axis and diet: a systematic review for athletes.” Journal of the International Society of Sports Nutrition vol. 13 43. 24 Nov. 2016, doi:10.1186/s12970-016-0155-6
Baothman, Othman A et al. “The role of Gut Microbiota in the development of obesity and Diabetes.” Lipids in health and disease vol. 15 108. 18 Jun. 2016, doi:10.1186/s12944-016-0278-4
De Luca, F, and Y Shoenfeld. “The microbiome in autoimmune diseases.” Clinical and experimental immunology vol. 195,1 (2019): 74-85. doi:10.1111/cei.13158
Jenq, Robert R et al. “Intestinal Blautia Is Associated with Reduced Death from Graft-versus-Host Disease.” Biology of blood and marrow transplantation : journal of the American Society for Blood and Marrow Transplantation vol. 21,8 (2015): 1373-83. doi:10.1016/j.bbmt.2015.04.016
Cresci, Gail A, and Emmy Bawden. “Gut Microbiome: What We Do and Don’t Know.” Nutrition in clinical practice : official publication of the American Society for Parenteral and Enteral Nutrition vol. 30,6 (2015): 734-46. doi:10.1177/0884533615609899
Ghaisas, Shivani et al. “Gut microbiome in health and disease: Linking the microbiome-gut-brain axis and environmental factors in the pathogenesis of systemic and neurodegenerative diseases.” Pharmacology & therapeutics vol. 158 (2016): 52-62. doi:10.1016/j.pharmthera.2015.11.012
Naseribafrouei A, Hestad K, Avershina E, et al. Correlation between the human fecal microbiota and depression. Neurogastroenterol Motil. 2014;26(8):1155-1162. doi:10.1111/nmo.12378
Kang D-W, Park JG, Ilhan ZE, Wallstrom G, LaBaer J, Adams JB, et al. (2013) Reduced Incidence of Prevotella and Other Fermenters in Intestinal Microflora of Autistic Children. PLoS ONE 8(7): e68322. https://doi.org/10.1371/journal.pone.0068322
Lach, Gilliard et al. “Anxiety, Depression and the Microbiome: A Role for Gut Peptides.” Neurotherapeutics : the journal of the American Society for Experimental NeuroTherapeutics vol. 15,1 (2018): 36-59. doi:10.1007/s13311-017-0585-0
Barrington, William T, and Aldons J Lusis. “Atherosclerosis: Association between the gut microbiome and atherosclerosis.” Nature reviews. Cardiology vol. 14,12 (2017): 699-700. doi:10.1038/nrcardio.2017.169
Ochoa-Repáraz, Javier et al. “The Gut Microbiome and Multiple Sclerosis.” Cold Spring Harbor perspectives in medicine vol. 8,6 a029017. 1 Jun. 2018, doi:10.1101/cshperspect.a029017
Sivan, Ayelet et al. “Commensal Bifidobacterium promotes antitumor immunity and facilitates anti-PD-L1 efficacy.” Science (New York, N.Y.) vol. 350,6264 (2015): 1084-9. doi:10.1126/science.aac4255
Holscher, Hannah D. “Dietary fiber and prebiotics and the gastrointestinal microbiota.” Gut microbes vol. 8,2 (2017): 172-184. doi:10.1080/19490976.2017.1290756
Doron, Shira, and David R Snydman. “Risk and safety of probiotics.” Clinical infectious diseases : an official publication of the Infectious Diseases Society of America vol. 60 Suppl 2,Suppl 2 (2015): S129-34. doi:10.1093/cid/civ085
Piqué, Núria et al. “Health Benefits of Heat-Killed (Tyndallized) Probiotics: An Overview.” International journal of molecular sciences vol. 20,10 2534. 23 May. 2019, doi:10.3390/ijms20102534
Reis, Daniel J et al. “The anxiolytic effect of probiotics: A systematic review and meta-analysis of the clinical and preclinical literature.” PloS one vol. 13,6 e0199041. 20 Jun. 2018, doi:10.1371/journal.pone.0199041
Dale, Hanna Fjeldheim et al. “Probiotics in Irritable Bowel Syndrome: An Up-to-Date Systematic Review.” Nutrients vol. 11,9 2048. 2 Sep. 2019, doi:10.3390/nu11092048
Aktuelle Beiträge zum Thema Mikrobiom
Leckere Winterheißgetränke
Welche Heißgetränke sind bei Fructoseintoleranz und Histaminintoleranz erlaubt? Die Winterzeit bringt viele leckere Heißgetränke mit sich. Besonders auf den Weihnachtsmärkten gibt es Höhepunkte wie Glühwein, Punsch oder Gewürztee. Aber auch zu Hause sind heiße Getränke mit oder ohne Alkohol sehr beliebt. Allerdings können Mehr lesen!
Gesunde Darmflora und ein gesundes Immunsystem sind entscheidend
Hilfreiche Bakterienkulturen und Mikroorganismen bei Fructose- und Histaminintoleranz Der menschliche Darm hat normalerweise eine Länge von etwa sechs bis neun Metern. Seine Oberfläche ist so groß wie zwei Tennisplätze. Der Darm ist somit das größte Organ im menschlichen Körper. Durch seine Beschaffenheit kann Mehr lesen!
Das Immunsystem benötigt für gute Arbeit viele Bauteile
Wie Vitamine, Mineralstoffe und Spurenelemente die Immunabwehr stärken Von Dr. Evelyn Zientz Kennen Sie den Spruch, dass ein Schnupfen ohne Behandlung sieben Tage dauert und mit eine Woche? Diese alte Weisheit hat mittlerweile ihre Gültigkeit verloren. Denn es ist wissenschaftlich erwiesen, dass hoch Mehr lesen!
Wie stärken Probiotika die Abwehrkräfte?
Darmbakterien und das Immunsystem Von Dr. Evelyn Zientz Das Darm-Mikrobiom spielt eine wichtige Rolle bei der Entwicklung eines funktionsfähigen Immunsystems nicht nur bei Neugeborenen. Auch in späteren Lebensphasen sind kommensale Darmbakterien (= in Eintracht mit dem Wirt lebende) immens wichtig für ein gut Mehr lesen!
Rotwein, Fisch und Sonne bei chronisch entzündlichen Darmkrankheiten
Darmflora und CED Unser Darm-Mikrobiom ist im Idealfall eine artenreiche Gesellschaft von Bakterien und anderen Mikroorganismen, wobei die Bakterien die überwiegende Mehrheit der Darmbewohner stellen. Das Darm-Mikrobiom ist nicht nur Ballast, den wir eben mit uns herumtragen. Seit es das Interesse der mikrobiologischen Mehr lesen!
Muskeln und das Mikrobiom
Wie die Darmflora Kraft und Ausdauer beeinflusst Von Dr. Evelyn Zientz Wir sind schon ziemlich toll, aber ohne unser Mikrobiom sind wir nichts. Die Mikrobiologie als Forschungsrichtung der Biologie gibt es seit gut 300 Jahren. Sie entstand mit der Entdeckung der Mikroorganismen durch Mehr lesen!
Wechselwirkung zwischen Arzneimitteln und Mikrobiom
Darmbakterien speichern Medikamentenwirkstoffe Von Dr. Evelyn Zientz Wenn wir Medikamente einnehmen, behandeln wir damit nicht nur uns, sondern auch das Mikrobiom in unserem Darm. Bei einer Antibiotikabehandlung ist uns der Zusammenhang schon lange bewusst. Aber auch andere Medikamente gehen Wechselwirkungen mit den Darmbakterien Mehr lesen!
Dank Corona haben Säuglinge es schwer, ein gesundes Darm-Mikrobiom aufzubauen
Auswirkungen von Corona-Maßnahmen und Covid-19 auf Neugeborene und Babys Von Dr. Evelyn Zientz Kinder kommen bei Covid-19 sehr glimpflich davon. Sie erleben in der Regel einen sehr milden Verlauf und oft zeigen sie gar keine Symptome. Eine weitere gute Nachricht ist, dass die Mehr lesen!
Sorbit, Aspartam & Co
Künstliche Süßstoffe – Fluch oder Segen? Von Dr. Evelyn Zientz Wir lieben süßen Geschmack, aber zu viel Zucker ist nicht gesund. Was ist die Entdeckung künstlicher Süßstoffe dann doch für ein Segen. Dank ihr können wir nach Herzenslust unserem Hunger nach Süßem nachgeben, Mehr lesen!
Das menschliche Virom
Viren als Bestandteil des gesunden Mikrobioms Von Dr. Evelyn Zientz Das Darm Mikrobiom ist aktuell in aller Munde und seine weitreichende Wirkung auf die Gesundheit seines Wirtes wird zurzeit intensiv erforscht. Ständig werden neue Zusammenhänge zwischen der Gesundheit unserer Organe und der Beschaffenheit Mehr lesen!